PRINCIP
Palivové články jsou obecně definována jako elektrochemická zařízení. Jejich funkcí je přeměna vodíku (palivo) a kyslíku (okysličovadlo) na energii elektrickou. Tento galvanický článek obsahuje dvě elektrody, které jsou odděleny jakousi membránou, případně mohou být odděleny též elektrolytem. Ke kladné elektrodě přivádíme palivo (vodík), k záporné elektrodě přivádíme oxidační činidlo (kyslík). Na kladné elektrodě (anodě) vznikají elektrony, které proudí přes vnější elektrický obvod k záporné elektrodě (katodě), díky čemuž nám začne vznikat elektrický proud.
Palivový článek může teoreticky pracovat nepřetržitě, dokud není přerušen přívod paliva nebo okysličovadla k elektrodám.
Existuje mnoho kombinací paliva a okysličovadla. Např. kyslíko-vodíkový článek používá vodík jako palivo a kyslík jako okysličovadlo, přičemž jako odpad produkuje čistou vodu. Jiné články užívají jako paliva uhlovodíky a alkoholy. Místo čistého kyslíku se jako okysličovadla může použít například vzduch, chlór nebo oxid chloričitý.
Elektrody mohou být zhotoveny z uhlíku (nanotrubičky), nebo z různých kovů. Vyšší účinnosti se může dosáhnout potažením katalyzátorem, kterým může být například palladium, nebo platina.
Jako elektrolyt mohou sloužit různé kyseliny (převážně H3PO4) nebo zásady (nejčastěji KOH), keramiky nebo membrány. U specifických palivových článků se používá jako elektrolyt plyn pod vysokým tlakem. Dnes nejpoužívanějším elektrolytem je KOH, který byl použit už u článků v projektu Apollo, jehož nevýhodou však je, že se oxidovadlo musí čistit od CO2, aby nedocházelo k reakci oxidu uhličitého s elektrolytem, neboť vzniklý uhličitan draselný by přestal plnit funkci elektrolytu.
Vznikající elektrické napětí je teoreticky okolo 1,23 voltu a závisí na typu paliva a kvalitě článku. U dnes nejpoužívanějších článků dosahuje nejčastěji napětí 0,5 - 0,95 V. Aby se dosáhlo vyššího napětí, zařazuje se více palivových článků do série. Velikost proudu závisí na ploše článku, dnes komerčně dostupné články poskytuji přibližně 0,5W/cm².
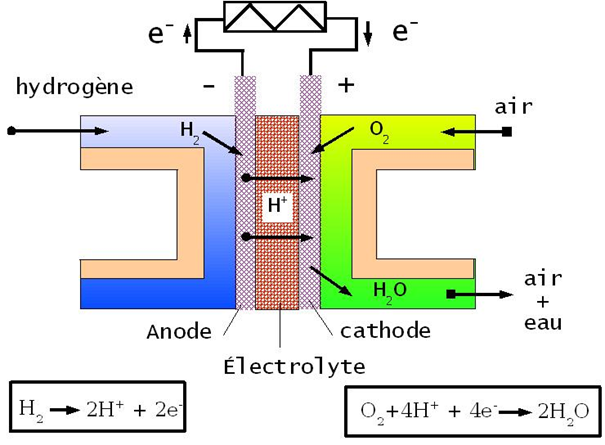
Obr. Schematické vyjádření dějů v palivovém článku
zdroj: https://cs.wikipedia.org/wiki/Palivový; článek
Palivo se na anodě katalyticky oxiduje na kationty (například vodík na H+), které přechází přes membránu nebo do elektrolytu. Uvolněné elektrony jsou navázány anodou a putují směrem k elektrickému spotřebiči. Vzhledem k zápornému náboji elektronů teče elektrický proud v opačném směru, tedy od katody (+) přes elektrický spotřebič k anodě (−). Na katodě se oxidační činidlo redukuje na anionty (například kyslík na O2−), a ty se pak slučují s kationty (v případě vodíku a kyslíku na vodu).